МЕМБРАННИЙ ПОТЕНЦІАЛ — різниця потенціалів, яка утворюється між розчинами електролітів, роз’єднаних мембраною, проникною для іонів. Мембранна система має такий вигляд:
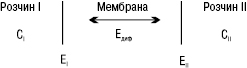
М.п. визначається рівнянням: ЕМ=ЕІІ — ЕІ + Едиф, де ЕІ і ЕІІ — потенціали Доннана на межі поділу мембрана — розчин І або ІІ відповідно; Едиф — внутрішній дифузійний потенціал мембрани. Для мембрани, крізь яку проникають катіони та аніони, значення М.п. описується рівнянням: ЕМ=RT/nF(t+-t–) ln CII/CI, де t+, t– — кількість переносу катіона та аніона відповідно; CI, CIІ — концентрації електроліту в розчинах І та ІІ відповідно. У разі якщо t+ = t– = ½, ЕМ=0. Для мембрани, через яку проникають лише катіони або аніони, рівняння мають такий вигляд:
 або
або  ,
,
де n+, n– — заряд катіона і аніона відповідно; а+, а– — активність катіона і аніона відповідно. Якщо у фазі мембрани присутні фіксовані заряди, напр. іоногенні групи з концентрацією X—, то рівняння для ЕМ значно ускладнюються. Тільки у трьох випадках вони мають просту форму:
1)  , тоді
, тоді  ;
;
2)  , тоді
, тоді  ; або
; або  ;
;
3)  , тоді
, тоді  .
.
М.п. також утворюється на межі поділу двох розчинників, які не змішуються, але мають загальний іон. У таких системах межа поділу відіграє роль мембрани, а М.п. описується рівнянням, аналогічним за формою рівнянню Нернста:  , де
, де  – різниця стандартних потенціалів загального іона у розчинниках І та ІІ, які не змішуються; аІ, аІІ — активність загального іона у розчинниках І та ІІ відповідно. Мембранним процесам і М.п. належить важлива роль у біології та медицині; вони лежать, зокрема, в основі розробки мембранних (іоноселективних) електродів, які використовуються в аналізі ЛП.
– різниця стандартних потенціалів загального іона у розчинниках І та ІІ, які не змішуються; аІ, аІІ — активність загального іона у розчинниках І та ІІ відповідно. Мембранним процесам і М.п. належить важлива роль у біології та медицині; вони лежать, зокрема, в основі розробки мембранних (іоноселективних) електродів, які використовуються в аналізі ЛП.
Никольский Б.П., Мастерова Е.А. Ионоселективные электроды. — Л., 1980.
