Альдегіди (франц. aldehyde, араб. al kohol — найвищий, найтонший + лат. dehyd (rogenatum) — органічні сполуки, які містять у своєму складі альдегідну групу:
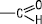
Загальна формула
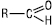
За природою вуглеводневого радикала Аальдегіди поділяють на аліфатичні (насичені та ненасичені), аліциклічні, ароматичні та гетероциклічні. У номенклатурі А. вживають тривіальні та систематичні назви. Тривіальні назви походять від назв кислот, на які вони перетворюються при окисненні. За замісною номенклатурою IUPAC назви А. утворюють від назв вуглеводнів з тією самою кількістю атомів карбону в головному ланцюзі (враховуючи альдегідну групу), додаючи суфікс -аль. Напр. НСНО — мурашиний альдегід, формальдегід або метаналь; СН3СНО — оцтовий альдегід, ацетальдегід або етаналь. Ненасичені альдегіди: СН2=СНСНО — акролеїн або пропеналь; СН2=СН–СН2СНО — вінілоцтовий альдегід або бутен-3-аль. Ароматичні альдегіди: С6Н5СНО — бензальдегід або бензойний альдегід; С6Н5СН2СНО — фенілоцтовий альдегід; С6Н5СН=СНСНО — коричний альдегід або 3-фенілпропеналь; 2-НОС6Н4СНО — саліциловий альдегід, 2-гідроксибензальдегід або о-оксибензальдегід; СН3(НО)С6Н3СНО — ванілін, 4-гідрокси-3-метоксибензальдегід. Сполуки, які містять дві альдегідні групи, належать до діальдегідів. Найпростішим у цьому ряду є гліоксаль ОНС — СНО.
А. належать до реакційноздатних речовин. Вони легко вступають в реакції приєднання, заміщення та конденсації. Внаслідок полярності
![]()
групи А. вступають в реакції приєднання (АN). При взаємодії з HCN утворюють оксинітрили:
RCHO + HCN ⇒RCH(OH)CN
Продуктами приєднання NaHSO3 є бісульфітні похідні А.:
RCHO + NaHSO3 →RCH(OH)SO3Na
При розчиненні у воді А. утворюють гідратні форми, як правило, нестійкі:
RCHO + H2O  RCH(OH)2
RCH(OH)2
При взаємодії А. зі спиртами утворюються напівацеталі та ацеталі (в присутності мінеральної кислоти):
RʹOH; H+
RCHO + RʹOH  (RCH(OH)ORʹ
(RCH(OH)ORʹ  RCH(ORʹ)2
RCH(ORʹ)2
Для А. характерні реакції заміщення оксигену в альдегідній групі. Ці реакції відбуваються за механізмом приєднання–відщеплення. При взаємодії з гідроксиламіном вони утворюють альдоксими:
RCHO + NH2OH → RCH = N — OH + H2O,
з гідразином — гідразони:
RCHO + H2NNH2 →RCH = N — NH2 + H2O
До реакцій заміщення належить реакція взаємодії А. з PC5 з утворенням гемінальних дигалогенопохідних вуглеводнів:
RCHO + PCl5 →RCHCl2 + POCl3
А. вступають в реакції конденсації. Альдольна та кротонова конденсації відбуваються в присутності каталітичної кількості лугу:
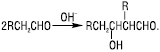
Продуктами альдольної конденсації є альдолі (β-оксиальдегіди) — сполуки, які містять альдегідну групу та спиртовий гідроксил. При нагріванні альдолів відщеплюється молекула води й утворюється α,β-ненасичений альдегід. Ця реакція відома під назвою «кротонова конденсація»:
![]()
А. легко окиснюються та відновлюються. Окиснення зумовлює утворення кислот без зміни вуглецевого скелета. Реакцію окиснення А. аміачним розчином нітрату срібла (реактив Толленса) і сумішшю розчинів сульфату міді з лужним розчином калійнатрієвої солі винної кислоти (реактив Фелінга) використовують в аналітичній практиці для виявлення альдегідної групи. При відновленні А. утворюються первинні спирти.
Нижчі альдегіди здатні до полімеризації, яка відбувається за звичайних умов та прискорюється в присутності мінеральних кислот. При стоянні 40% водного розчину формальдегіду (формаліну) при T <9 °C утворюється параформ:
nHCHO + H2O →HOCH2(OCH2)nOH
Полімеризація оцтового альдегіду, залежно від умов, призводить до утворення двох циклічних продуктів паральдегіду (І) (20 °С) та метальдегіду (ІІ) (0 °С):
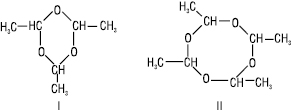
Паральдегід — рідина (Tкип 128 °С); метальдегід — тверда речовина, так званий сухий спирт, використовується як сухе пальне.
Для одержання А. застосовують кілька промислових методів. А. аліфатичного ряду отримують оксосинтезом (пряме приєднання СО та Н2 до алкенів):
![]()
Реакцію проводять при T 100–200 °С під тиском 100–200 атм. в присутності кобальтового або нікелевого каталізатора; реакцію з етиленом та пропіленом — у газовій фазі, а з більш складними алкенами (С3 — С20) — в рідкій.
Оцтовий альдегід одержують за допомогою реакції Кучерова (гідратація ацетилену в присутності солей Нg2+ та концентрованої Н2SO4):
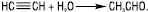
Мурашиний альдегід добувають термічним дегідруванням метанолу при T 600 °С над срібним каталізатором:
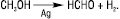
Найпростіший ненасичений альдегід — акролеїн у промисловості добувають методом окиснення пропілену:
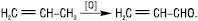
Для одержання ароматичних альдегідів найчастіше застосовують метод окиснення метилвмісних аренів у м’яких умовах, використовуючи такі окисники, як хрому (VI) оксид, мангану (IV) оксид та ін. Окиснення оксидом хрому проводять у присутності оцтового ангідриду:
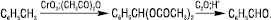
Важливе значення також має спосіб прямого введення альдегідної групи в ароматичне ядро (реакція Гаттермана — Коха):
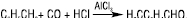
А. широко застосовують в синтезі ЛЗ, полімерів (поліформальдегіду, феноло- та сечовиноальдегідних смол), карбонових кислот, амінів, спиртів; у виробництві барвників, ароматичних сполук, пестицидів. Водний розчин формальдегіду (37–40%) з 6–15% метанолу (формалін) використовують як дезінфекційний засіб та консервант для анатомічних препаратів. Похідним формальдегіду є уротропін — сечогінна речовина, складова протизастудного препарату Кальцекс; застосовується для лікування захворювань нирок та ін.; у великих кількостях використовують у виробництві фенолоформальдегідних смол та вибухових речовин (гексогену). Ванілін є вихідною сполукою в синтезі протитуберкульозного препарату Фтивазид.
Вейнганд-Хильгетаг К. Методы эксперимента в органической химии. — М., 1962; Моррисон Р., Бойд Р. Органическая химия. — М., 1974; Общая органическая химия. В 12 т. / Под общ. ред. Д. Бартона, У.Д. Оллиса. — Т. 2. Кислородсодержащие соединения. — М., 1982.
