ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ (грец. heteros — інший + kyklos — коло) — органічні речовини, що містять цикли, до складу яких, крім атомів карбону, входять один або декілька атомів інших елементів (гетероатомів).
Г.с. класифікують залежно від розміру циклу (три-, чотири-, п’яти-, шести- та семичленні гетероцикли), природи і числа гетероатомів (кисне-, азот-, сірковмісні), конденсовані Г.с., також ступеня насиченості циклу (насичені, ненасичені та ароматичні). Для Г.с. застосовують тривіальні та систематичні назви. Тривіальні назви визначені номенклатурою IUPAC і переважно є більш вживаними. При побудові систематичних назв гетероциклів номенклатурними правилами IUPAC враховуються природа та число гетероатомів, розмір циклу та ступінь його насиченості. Природу гетероатома відображають у префіксі, розмір циклу — в корені, міру насиченості — у суфіксі назви. Для позначення гетероатомів використовують префікси окса- (О), тіа- (S) і аза- (N). Розмір циклу позначають коренями -ір- (три-), -ет-, -єт- (чотири-), -ол- (п’яти-), -ин- (шести-), -еп- (семичленний), ступінь насиченості — суфіксами -идин, -ідин (насичений цикл з атомом нітрогену), -ан (насичений цикл без атома нітрогену), -ин, -ін (ненасичений цикл). У назві гетероциклів із максимально можливою кількістю подвійних зв’язків у циклі суфікс не вказують. Для частково гідрованих сполук використовують префікси дигідро-, тетрагідро- з позначанням номерів атомів, до яких приєднаний гідроген. Якщо атом гідрогену приєднаний тільки до одного атома, то в назві позначається літера Н і номер гідрованого атома. У шести- і семичленних азотвмісних гетероциклах повна насиченість циклу позначається префіксом пергідро-. Число однакових гетероатомів позначають у назві множинними префіксами ди-, три-, тетра- і т.д. Якщо гетероцикл містить кілька різних гетероатомів, то називають їх у певній послідовності: окса-, тіа-, аза-. Приклади тривіальних* та систематичних назв деяких гетероциклів: етиленоксид* (оксиран) (І), етиленімін* (азиридин) (ІІ), етиленсульфід* (тіїран) (ІІІ), оксетан (IV), азетидин (V), тієтан (VI), фуран* (оксол) (VII), пірол* (азол) (VIII), тіофен* (тіол) (IX), піразол* (1,2-діазол) (X), імідазол* (1,3-діазол) (XI), тіазол* (1,3-тіазол) (XII), оксазол* (1,3-оксазол) (XIII), піридин* (азин) (XIV), піридазин* (1,2-діазин) (XV), піримідин* (1,3-діазин) (XVІ), піразин* (1,4-діазин) (XVІІ), азепін (XVІІІ):
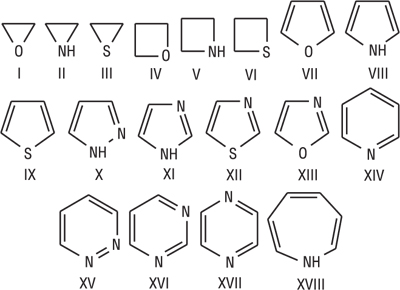
Нумерацію атомів у Г.с. починають з гетероатома і проводять у такому напрямку, щоб замісники отримали менші номери. У п’ятичленних і шестичленних Г.с. з одним гетероатомом атоми карбону іноді позначають грецькими літерами α, β, та γ. У Г.с. із кількома рівноцінними гетероатомами нумерацію здійснюють таким чином, щоб гетероатоми отримали найменші номери. Для деяких Г.с. існує окремий порядок нумерації. Для конденсованих Г.с. застосовують тривіальні* та систематичні назви. За систематичною номенклатурою назви конденсованих Г.с. утворюють, використовуючи як родоначальні структури тривіальні назви гетероциклів. При побудові назв конденсованих систем, які складаються з одного гетероциклічного та одного або двох бензольних ядер, до назви гетероциклу приєднують префікс бенз-(бензо-) або дибенз-(дибензо-) з позначенням буквами а, b, c, d тощо зв’язку гетероциклу, вздовж якого відбувається конденсація. Позначення зв’язків починають від гетероатома. Якщо конденсована система складається з двох гетероциклів, за основу назви беруть назву циклу, більшого за розміром; при однакових розмірах — циклу з більшою кількістю гетероатомів. Якщо за першими двома критеріями цикли рівнозначні, то азотвмісний цикл має перевагу над кисневмісним, а останній — перед сірковмісним. За допомогою літер позначають зв’язок основного циклу, який є спільним для обох циклів, а за допомогою цифр — спільний зв’язок другого циклу з основним. Напр., індол* (бензо[b]пірол) (ІХХ), хінолін* (бензо[b]піридин) (ХХ), акридин* (дибензо[b,e]піридин) (ХХІ), піроло[2,3-b]піридин (XXIІ), піридо[2,3-d]піримідин (XXІІІ):
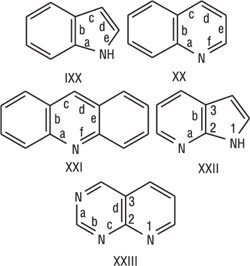
За хімічними властивостями три- та чотиричленні Г.с. — реакційноздатні сполуки (вплив кутового і торсійного напруження циклів, наявність полярних зв’язків). При дії електрофільних і нуклеофільних реагентів відбувається розрив гетероатом-вуглецевого зв’язку та приєднання молекули реагенту за місцем розриву циклу. Для азотвмісних три- та чотиричленних Г.с. характерні властивості вторинних амінів. Реакційна здатність п’ятичленних Г.с. з одним гетероатомом визначається наявністю в їх структурі циклу з π-електрононадлишковою ароматичною системою (у спряження з π-електронами подвійних зв’язків вступає неподілена пара електронів гетероатома, утворюється замкнена кон’югована система, в якій число узагальнених π-електронів відповідає правилу Гюккеля (4n + 2). Вони вступають у характерні для ароматичних сполук реакції електрофільного заміщення (нітрування, сульфування, ацилювання, галогенування). Враховуючи ацидофобність фурану, піролу та індолу, реакції проводять у лужному середовищі або використовують комплекси електрофільних реагентів з лугами. Електронна густина п’ятичленних Г.с. з двома гетероатомами (див. Азоли) розподілена нерівномірно, це визначає напрямок дії електрофільних та нуклеофільних реагентів. Азоли — стабільні сполуки, виявляють здатність до таутомерних перетворень та утворення міжмолекулярних водневих зв’язків. Шестичленні Г.с. з одним гетероатомом — π-дефіцитні ароматичні системи. За участю гетероатома утворюють солі та донорно-акцепторні комплекси. Реакції електрофільного заміщення відбуваються за жорстких умов. З нуклеофільними реагентами легко утворюють продукти заміщення (аміно- та гідроксипохідні). Для шестичленних Г.с. із двома гетероатомами реакції електрофільного заміщення можливі за наявності електродонорного замісника, реакції нуклеофільного заміщення проходять легко.
Г.с. поширені у природі. Деякі Г.с. містяться у кам’яновугільній та деревній смолі. Входять до складу природних речовин (хлорофіл, гемоглобін, вітаміни, алкалоїди, нуклеїнові кислоти, ферменти та ін.). Багато Г.с. мають високу біологічну активність, тому більше половини всіх лікарських речовин містять у своїй структурі гетероциклічні фрагменти. З використанням Г.с. пов’язано утворення напрямків у терапії різноманітних захворювань: препарати фенотіазинового і діазепінового ряду, пеніцилінові та пуринові антиметаболіти застосовують у хіміотерапії пухлин, інгібітори АПФ — в кардіології, ациклогуанозин та азидотидин — у лікуванні вірусних інфекцій та ін.
Джилкрист Т. Химия гетероциклических соединений. — М., 1996; Джоуль Дж., Миллс К. Химия гетероцикличных соединений. — М., 2004; Общая органическая химия. В 12 т. / Под общ. ред. Д. Бартона и У.Д. Оллиса. Т. 8. Азотсодержащие гетероциклы / Под ред. П.Г. Сэммса. — М., 1985; Т. 9. Кислородсодержащие, серусодержащие и другие гетероциклы / Под ред. П.Г. Сэммса. — М., 1985; Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия / Под общ. ред. В.П. Черных. — 2-е изд. — Х., 2007.
